| 苏州长留净化科技有限公司 | |
 |
0512-62387955 0512-66985755 |
 |
0512-67064265 |
 |
全国热线 400-990-6761 |
 |
changliu008@126.com |
 |
苏州吴中经济开发区东方大道1210号 |
GMP厂房解决方案
药品是特殊商品,它关系到人民用药安全有效和身体健康的大事。质量好的药品,可以治病救人;劣质的药品,轻则延误病情,重则致人于死地,所以对药品的质量要求,非同小可。
解决方案
具体布局首先应该了解当地常年的风向状况,即当地风向频率图,然后考虑划分区域。一般药厂区域划分为生产区、行政区、生活区。生产区包括生产车间、库房、通用工程(也有通用工程单分区)。
生产车间要考虑所建车间的性质,洁净级别的要求。生产针剂的车间对环境空气洁净度要求,且车间不排放有毒有害气体和粉尘,一般布置于常年的上风向。而生产
片剂、颗粒剂的车间由于产生粉尘,一般布置在常年的下风向。通用工程包括变配电室、锅炉房等供能设施,布置于生产车间的下风向。
通用工程包括变配电室、锅炉房等供能设施,布置于生产车间的下风向。 行政区包括供销部门和管理部门,一般布置于厂区最明显且交通方便的地方,目的是便于对外接洽业务,一般布置于厂正门附近。生活区一般包括食堂、宿舍、娱乐
设施。要求空气不受污染,不受噪音干扰等。绿化是一项很重要的部分,不仅是为了美化厂容厂貌,而且也可以保持厂区整洁无尘。绿化应以种草坪为主。不得种植 产生花絮、花粉的花卉和树木。一般要求绿化面积占厂区面积的30%以上。
如何建设符合GMP要求的生产车间这个问题相当复杂,因为医药生产剂型多,而且同一剂型不同品种生产具体要求也有所不同,具体应该从以下几方面考虑。
厂房的工艺设计
按产品的工艺流程确定工艺布局,工艺布局应按工序先后顺序衔接合理,避免交叉迂回及人、物混杂。人员及物料均应有各自的出入口,尽量人流物流分开。
洁净厂房应按洁净级别合理布局,洁净级别高的工序应设在中心,并设置相应的辅助措施,包括清洗、更衣等措施。
厂房的建筑类型
厂房的建筑设计首先考虑厂房设计的类型,即单层厂房还是多层厂房。一般建单层大跨度厂房为多。其优点是:单层厂房工艺布局比多层厂房更易合理;灵活性较强,便于生产品种的更新和工艺流程变更时工房进行改造;便于设备安装和公用管线的安装。
厂房的洁净要点
洁净厂房的洁净级别,我国现执行的《洁净厂房设计规范》GB73-84,原则上采用国际上多数国家通用的工业洁净室空气洁净度等级,洁净级别划分为3个等级。

要达到以上3个级别设计:
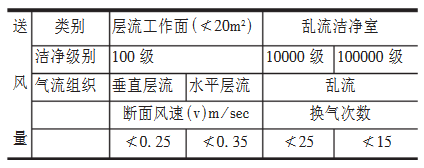
1、气流组织,一般100级采用垂直层流、水平层流,10000级和100000级采用乱流(一般为顶部送风,墙下部设回风口)。
2、压差,洁净级别高区域对相邻洁净级别低的区域呈正压。
3、送风量,送风量是洁净厂房达到级别要求的重要因素,设计时根据实际情况应留有一定系数。
4、新鲜空气量,新风量一般占送风量70%。
厂房设计思路
1、平面图上要划分洁净区和辅助区,人员进入洁净区必需先通过辅助区。辅助区包括更衣室,缓冲间,人流方向应由低洁净级别区到高洁净级别区。
2、为了节约能源,洁净区在满足生产的情况下空间不宜过大,高度应尽量降低,一般在2.5米左右。
3、不同洁净级别的洁净室之间结合部应设防尘设施,如气闸、传递窗等。
4、洁净区和非洁净区的间隔窗户为双层密闭窗,门应严密。
厂房建筑过程:
要使新建的厂房符合GMP要求,厂房建筑过程中的质量控制甚为重要。土建中厂房结构要求由土木建筑技术人员去管理和控制,下面谈谈和车间GMP要求有关的问题。
1、墙面要求平整光滑,不留尘土易于清洗,所以墙面一般用高品质的防水涂料进行涂刷。洁净级别高的厂房墙面可贴彩钢板材料,内墙面之间和天花板的交界处应做成园角。
2、隔断材料,一般采用铝合金材料和聚苯乙烯彩钢板材料。特别是有洁净级别的厂房均采用彩钢板材料。这种材料的优点是重量轻,光亮平整,易清洗,施工简便,易于生产工艺变更时工房改造。
3、对地面材料要求强度高,应耐磨损,光滑平整,易清洗,一般是现制水磨石地面,对于洁净级别要求高的厂房地面一般采用环氧树脂地面。地面排水:普通厂房采用普通地漏,有洁净级别的厂房应采用洁净地漏,洁净级别高的厂房地面不设地漏。
4、窗户一般采用钢窗和铝合金窗户,窗户和墙面交接处应做成斜角,洁净级别高的窗子应做成固定窗,窗玻璃和墙面应做成同一平面,防止窗沿积尘,且易于清洗。
制药设备
制药设备在药品生产中起着重要的作用,产品质量的好坏在很大程度上决定于设备完善的程度。设备要符合生产工艺要求,达到国家规范标准,设备主要考 虑以下几方面
设备的选型
①设备应适合生产品种的工艺要求,其容量应适合批量生产能力。
②设备结构应简单,便于操作,易于拆装、清洗、灭菌和维修。
③设备传动部分应密闭良好,防止药物污染。
④粉碎、过筛、混合、压片、包衣等生产设备应安装有效的捕尘装置。
⑤设备的各种计量、检测控制仪表其适用范围和精度应符合生产要求,并达到国家规定的计量标准。
设备的材质
设备与加工物品接触面应光滑平整,易清洗消毒,化学抗蚀性高,不与加工物品产生改变其成份、含量等反应。
设备的布局
①设备应按工艺流程合理布局,使加工物料按同一方向流动,避免重复往返。
②设备应有足够的操作空间,占有面积合理。一些设备可按移动方式或半固定方式安装,以便于清洗和维修。
—洁净区的设备为防止相互污染,宜分室安装,一机一室。
—跨越不同洁净级别区的设备要采取措施使洁净级别高的区域不受污染。
③固定安装的管线应按《医药工业设备及管路涂色规定》喷涂不同颜色,应有流向标志。
有洁净级别的厂房、管道应安装在技术隔层和技术竖井内,避免和减少外露。
设备的验证
生产工艺重要控制点的设备,例如热压灭菌设备,用于分装无菌制剂的设备,除了其选择安装、使用应与药品生产要求相适应以外,在安装后应进行验证, 并制定验证周期定期验证。
药厂的竣工验收
药厂GMP验收应包括多方面,包括人员配备、厂房(设备)、卫生、生产管理、质量保证等方面,仅就厂房建设而言,归纳为以下几点。
①按厂区布局→厂房建筑装修→制药设备逐次进行竣工验收。
②厂房建筑装修应按产品生产工艺要求进行验收。
③洁净厂房应按照国家行业标准JGJ71-90《洁净室施工及验收规范》进行验收。首先进行工程竣工验收,再进行综合性能全面评定。两者都必须对
洁净室进行性能检测。
(1)工程竣工验收
即应对各部分工程做外观检查,单机试运转,系统联合试运转。并在空态或静态条件下对洁净室的性能进行检测和调整,以及对有关
施工检查记录进行审查。
a外观检查项目包括:各种管道、风道、净化空调设备的安装是否正确严密,高效、中效过滤器安装合理、密封,洁净室墙面、地面、天花板应光滑平整,门窗严密。
b单机试运转是指对空调器(制冷,加热系统)、局部净化设备及其它有试运转要求的设备分别进行试运转,审查是否符合有关技术规定
c系统联合试运转是在单机试运转合格后,进行各项设备部件联动运转,审查是否符合技术要求。
(2)综合性能全面评定
综合性能全面检测的方法及评定标准应符合JGJ71-90《洁净室施工和验收规范》。检测包括以下方面:洁净度级别、送 风量、排风量、截面风速、浮游菌和沉降菌、温度和湿度等。
另外在竣工验收时施工单位应递交下列文件:
a.设计变更洽商和竣工图。
b.主要材料、设备、仪表出厂合格证和检验文件。主要建筑材料还应有当地建 设工程质量监督站的检验文件。
c.单位工程、分次分部工程质量检验评定书、隐蔽工程记录(包括照片)。d.设备的试运转记录、管道压力试验记录。
厂房竣工验收合格后,建设方和施工方签订建设工程保修合同。
苏州长留净化科技有限公司为药厂客户提供完整的生物安全柜的3Q认证文件和检测,我们配备了专业的检测设备和工程师,提供安装确认(IQ)服务及文件,运行确认(OQ)服务及文件,并可以协助用户完成性能确认(PQ)服务及文档的相关内容。
物安全柜主要检测内容包括:菌落数量采集、风速检测、气流模式检测、滤膜检漏(气溶胶)扫描、空气颗粒扫描、光照度检测。

电话:0512-62387955 地址:中国·江苏省·苏州市吴中经济开发区东方大道1210号
苏ICP备10216823号-7 友情链接:PC板